УДК: 616.36-002.2:[616.98:578.828.6-HIV]-085:281.8
Год издания: 2013
Противовирусная терапия хронического гепатита С у ВИЧ-инфицированных пациентов
Матиевская Н.В., Цыркунов В.М.
Рубрики: 76.29.34, 76.29.50
Гродненский государственный медицинский университет
Тема НИР: «Разработать критерии патоиммуноморфологической диагностики поражений печени различной этиологии у ВИЧ-инфицированных пациентов».
Сроки выполнения НИР: II кв. 2011 г. — IV кв. 2015 г.
Научный руководитель: д-р мед. наук, проф. В.М. Цыркунов.
Соисполнители: ГУ «Республиканский научно-практический центр эпидемиологии и микробиологии».
Источник финансирования: госбюджет.
Цель - оценить результаты и переносимость противовирусной терапии ХГС у ВИЧ-инфицированных пациентов СТ и ПГ ИФН альфа-2b.
В настоящее время противовирусная терапия (ПВТ) ВГС-инфекции проводится лекарственными средствами рекомбинантным интерфероном-альфа (ИФН-α), который представлен стандартными «короткими» ИФН (СТ ИФН) и пегилированными ИФН (ПГ ИФН), как правило, в комбинации с рибавирином (РИБ). Эффективность противовирусной терапии на основании ИФН-α остается недостаточно эффективной и в целом составляет около 50%. Клиническое применение ПГ ИФН у ВИЧ-инфицированных пациентов сталкивается с высокой частотой досрочного прерывания лечения из-за возникновения серьезных нежелательных явлений (НЯ) терапии, развивающихся у 12-51% пациентов. В то же время результаты международных исследований демонстрируют эффективность СТ ИФН, сравнимую с ПГ ИФН при 2 и 3 генотипах ВГС, наличие у них меньшей частоты НЯ, в т. ч. прогрессирования иммунносупрессии. Кроме того, важным является более низкая стоимость СТ ИФН, что делает его более доступными для использования ВИЧ-инфицированными пациентами.
Под наблюдением находилось 44 ВИЧ-инфицированных пациента, получавших ПВТ ХГС СТ ИНФ и ПГ ИФН. Диагноз ВИЧ-инфекции верифицировали методом ИФА и иммуноблотом. Для определения клинической стадии ВИЧ-инфекции использовали классификацию ВОЗ (2006). Диагноз ВГС-инфекции у всех пациентов в группе был подтвержден обнаружением РНК ВГС. Для определения РНК ВГС и генотипа ВГС использовался метод ПЦР (Амплисенс, РФ). Вирусная нагрузка (ВН) ВИЧ (РНК) определялась методом ПЦР в режиме real time (Амплисенс, РФ), нетестируемый уровень ВН ВИЧ был менее 500 кп/мл. Характеристика пациентов представлена в табл. 1.
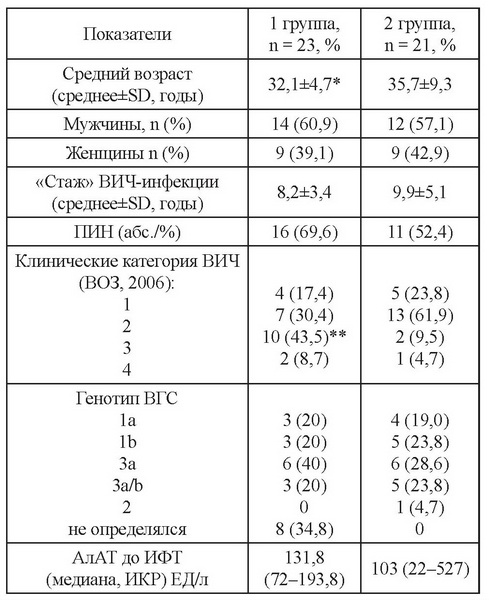
Примечание: * - p<0,05, Mann-Whitney U Test; ** - p<0,05, Тест х2; ИКР - интерквартильный размах.
Всем пациентам в группах рекомендовалась ПВТ ХГС в виде комбинации ПГ ИФН и РИБ. В связи с недоступностью ПГ ИФН для части пациентов 23 из них пролечены с помощью СТ ИФН. Наблюдаемые пациенты были разделены на 2 группы: 1 группа - 23 пациента, получавшие ПВТ ХГС средствами рекомбинантного СТ ИФН альфа-2b и РИБ, 2 группа - 21 пациент, получавшие терапию средствами ПГ ИФН альфа-2b и РИБ.
Сокращение рекомендуемых 48-недельных курсов терапии, а также монотерапии лекарственными средствами с помощью ИФН-α было связано с отсутствием эффективности от ПВТ, развитием НЯна ПВТ, отказом пациентов от лечения и отсутствием средств у пациентов.
ПВТ ВГС-инфекции у большинства пациентов в обеих группах начиналась на фоне ВААРТ, при этом продолжительность ВААРТ до начала ПВТ ХГС у пациентов 2-й группы была больше (p<0,03). ПВТ ХГС как стартовая схема терапии ко-инфекции ВИЧ/ВГС (до назначения ВААРТ) была проведена у 10 (43,55) пациентов 1-й группы и у 4 (19,0%) - во 2-й группе. Присоединение ВААРТ на фоне проводимой ПВТ ХГС было выполнено у 2 пациентов 2-й группы в связи с прогрессированием ВИЧ-инфекции. Замена схем ВААРТ в ходе ПВТ ХГС была проведена у 9 (39,1%) пациентов в 1-й группе и у 7 (33,3%) - во 2-й группе (p>0,05). Причинами замены схем ВААРТ были развитие НЯ(анемия, возбуждение и др.), риск гепатотоксичности, а также прогрессирование иммуносупрессии на фоне ПВТ.
Препараты СТ ИФН пациентам 1-й группы назначались парентерально в дозе 3 млн МЕ 3 раза в неделю. ПГ ИФН альфа-2b во 2-й группе назначался в дозе 1,5 мг/кг 1 раз в неделю, РИБ - ежедневно в дозе 1000-1200 мг с учетом веса пациента. Временное снижение дозы РИБ или полная отмена в связи с развитием НЯи плохой переносимостью проведены у 5 (29,4%) пациентов 1-й группы и 13 (76,5%) - во 2-й группе (p>0,05).
Результаты ПВТ ко-инфекцией ВИЧ/ВГС оценивались по общепринятым критериям и представлены в табл. 2. Не установлено достоверных различий в частоте и характере вирусологического ответа (ВО) на ПВТ как в целом в группах, так и в зависимости от получения ВААРТ.
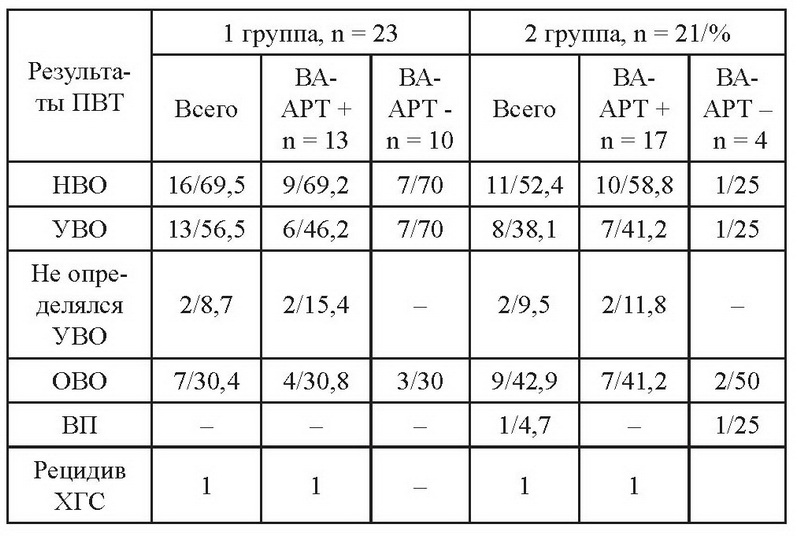
Примечание: НВО - вирусологический ответ к завершению терапии; ВП - вирусологический прорыв; УВО - устойчивый вирусологический ответ; ОВО - отсутствие вирусологического ответа.
Генотип ВГС считается одним из определяющих факторов в достижении ВО на ПВТ ХГС. В табл. 3 представлены результаты ПВТ ХГС у ВИЧ-инфицированных пациентов в зависимости от генотипа ВГС. Как видно из табл. 3, не выявлены достоверные различия в частоте НВО и УВО на ПВТ ХГС у пациентов с 1 и не 1 генотипом ВГС внутри групп, так и между сравниваемыми группами.
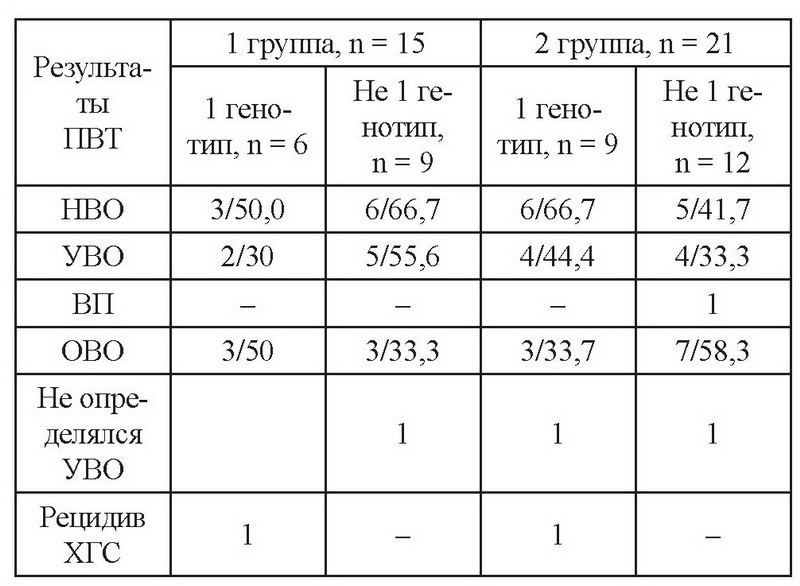
Примечание: ВО - вирусологический ответ; НВО - ответ к завершению терапии; УВО - устойчивый вирусологический ответ; ВП - вирусологический прорыв; ОВО - отсутствие вирусологического ответа.
При оценке результатов ИФН терапии в группах в зависимости от стадии фиброза печени и степени активности гепатита различий не обнаружено (p>0,05). Так, среди 7 пациентов 1-й группы с фиброзом 0 и 1 у 5 отмечен НВО, при этом у 3 зафиксирован УВО. Среди 4 пациентов 2-й группы с фиброзом 1 у 1 установлен НВО и УВО. У 1 пациента с фиброзом 3 в 1-й группе отмечен УВО. Среди 2-х пациентов с установленным фиброзом 3 во 2-й группе УВО зафиксирован у 1 пациента.
Одним из основных ограничений к широкому терапевтическому использованию лекарственных средств ИФН-α у ВИЧ-инфицированных пациентов является риск снижения CD4+T-лимфоцитов и усугубление иммуносупрессии. Динамика CD4+ Т-лимфоцитов и уровня ВН ВИЧ на фоне ПВТ в группах наблюдения представлена в табл. 4.
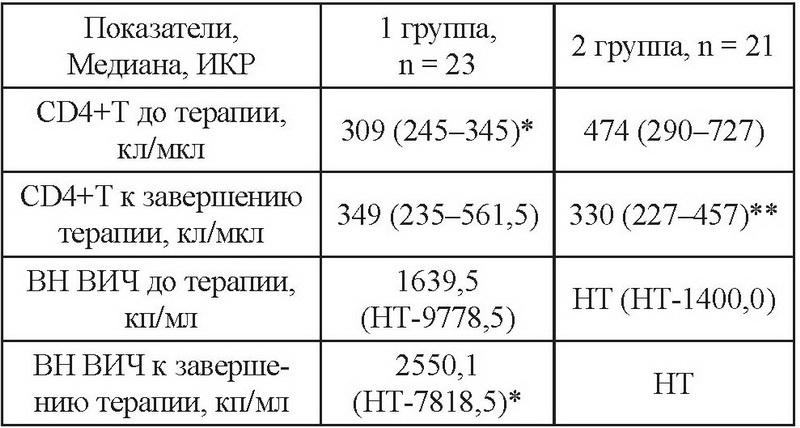
Примечание: * - p<0,05 при сравнении с группой 2, p<0,05, Mann-Whitney U Test; ** - p<0,05, при сравнении показателя до терапии и к завершению терапии во 2 группе, Wilcoxon Matched Pairs Test; ИКР - интерквартильный размах; НТ - нетестируемый уровень ВН ВИЧ (<500 кп/мл).
Исходный уровень CD4+Т до терапии в 1-й группе пациентов был ниже, чем во второй. К завершению терапии в 1-й группе отмечено некоторое повышение уровня клеток, в то время как во 2-й группе - достоверное снижение CD4+Т-лимфоцитов по сравнению с исходным уровнем, что указывает на более выраженный иммуносупрессивный эффект ПГ ИФН по сравнению со СТ ИФН. Уровни ВН ВИЧ до терапии не различались в группах пациентов, к завершению терапии ВН ВИЧ в 1-й группе несколько повысилась (p>0,05).
Наиболее распространенным НЯв 1-й группе пациентов был гриппоподобный синдром (ГПС), который исчезал через у 2-3 недели у большинства пациентов, у 4 пациенток повышение температуры тела до субфебрильных цифр сохранялось на протяжении ИФТ. Во 2-й группе у 9 пациентов отмечено повышение температуры длительностью от 1 до 3 дней после инъекции ПГ ИФН.
Депрессия в 1-й группе отмечена у 4 пациентов, которые в прошлом были наркопотребителями (17,4%). При этом депрессия, возбуждение, сонливость у 2 пациентов 1-й группы не требовали специализированной психиатрической помощи и отмены ИФТ. У 2 пациентов развилась выраженная депрессия, что привело к перерывам терапии в течение первых 3 мес. и полной отмене через 3 мес. лечения в связи с отсутствием ВО. Во 2-й группе депрессия отмечена у 7 пациентов, при этом 5 из них отказались от дальнейшей ПВТ.
Снижение массы тела, отмеченное у 4 пациентов в 1-й группе, было не более 5%, после завершения ПВТ вес быстро восстановился. Во 2-й группе снижение массы тела отмечено у 13 пациентов, при этом у 5 из них снижение было более 5%. У 2 пациенток 2 группы, ответивших на ПВТ, развилась липоатрофия, потребовавшая замены схем ВААРТ и досрочного прекращения ПВТ в одном случае, несмотря на достижение УВО. Гематологические сдвиги отмечены приблизительно с одинаковой частотой в группах.
Выводы. Стандартом ПВТ ХГС у ВИЧ-инфицированных пациентов является комбинированная терапия ПГ ИФН и РИБ. Как показывает практика, у столь сложной и неоднородной категории пациентов, какими являются пациенты с ко-инфекцией ВИЧ/ХГС, главным принципом при назначении и мониторинге ПВТ является индивидуальный подход как при выборе терапии, так и при индивидуальном прогнозировании эффективности ПВТ.
Область применения: инфекционные болезни, гепатология, клиническая медицина.
Рекомендации по использованию: дальнейшие исследования по разработке новых направлений в терапии коинфекции ВИЧ/ВГС.
Предложения по сотрудничеству: совместные исследования по иммунологии и разработке новых лекарственных средств в терапии ВИЧ/ВГС.