УДК: 616-002.4:616.336
Год издания: 2017
Морфологические особенности отключенной кишки у недоношенных детей с некротизирующим энтероколитом
Свирский А.А., Клецкий С.К., Севковский И.А., Махлин А.М., Мараховский К.Ю., Силина Е.В., Жук Е.Н.
Рубрики: 76.29.39
Республиканский научно-практический центр детской хирургии
Тема НИР: «Разработать и внедрить алгоритм оказания медицинской помощи новорожденным при некротизирующем энтероколите (НЭК)».
Сроки выполнения НИР: 05.01.2015 г. — 31.12.2017 г.
Научный руководитель: канд. мед. наук, доц. А.А. Свирский.
Источник финансирования: госбюджет.
Некротизирующий энтероколит (НЭК) - одно из самых тяжелых заболеваний периода новорожденности, сохраняющее высокий процент летальности (20-80%), особенно у недоношенных с экстремально низкой (ЭНМТ) и очень низкой массой тела (ОНМТ). Распространенность этой нозологии составляет от 5 до 10% у детей первого месяца жизни, находящихся в отделениях неонатальной реанимации. Одним из наиболее безопасных вариантов оперативного лечения, применяемых в хирургической стадии НЭК, является резекция измененного участка кишечника с выведением кишечных стом. Выхаживание новорожденных после объемных резекций кишки вызывает сложности и зависит от качества интенсивной терапии, энтерального питания, видов и способов его реализации. Большие потери по кишечной стоме могут привести к метаболическим нарушениям, требующим интенсивных затрат на лечение, и быть причиной различных клинических осложнений, ухудшающих прогноз заболевания. Поэтому выбор оптимального времени для выполнения операции по «закрытию» стом кишечника - один из факторов, создающих возможность адекватного нутритивного обеспечения, влияющего на психомоторное развитие ребенка, и в итоге - на результаты лечения пациентов с НЭК.
Цель - провести анализ морфологических изменений отводящего конца кишечной стомы у недоношенных новорожденных, перенесших НЭК, для определения оптимального времени операции по восстановлению непрерывности кишечника.
Проведен анализ архивного материала и биопсий в отделении детской патологии ГКПАБ г. Минска, 23 карт стационарных новорожденных, которые получали лечение НЭК в период с 2014 по 2016 г. в РНПЦ детской хирургии, и повторно поступали для выполнения операций по закрытию стом. Изучены акушерский анамнез, гестационный возраст, антропометрические параметры новорожденного, биохимические показатели крови, определяющие нутритивный статус пациента, объем первичных и вторичных оперативных вмешательств, тип стомирования (еюно-, илео-, колостома), время между открытием и закрытием стом.
Было установлено, что 87% пациентов родились раньше срока, и их средний гестационный возраст составил 33,5 недели (29-39). Масса тела при рождении в среднем составила 2062 г. (870-4180). Большинство матерей имело отягощенный акушерский анамнез, беременность протекала с различными инфекционными заболеваниями и осложнениями. Внутриутробное инфицирование установлено у 62% детей.
Проявление симптомокомплекса НЭК у новорожденных изучаемой группы чаще всего отмечено на 2-4-й неделе жизни. После диагностических мероприятий и констатации IIб-IIIб стадии заболевания дети переводились в хирургический стационар. В дальнейшем не было установлено статистически значимой зависимости влияния стадии НЭК на объем оперативного вмешательства и тяжесть послеоперационного периода.
Средний возраст новорожденных при первичном оперативном вмешательстве составлял 14 дней жизни (2-37, Ме - 13). Перфорация стенки в 56% случаев возникала в терминальном отделе подвздошной и куполе слепой кишки. Двухконцевая илеостома выведена у 78% пациентов. Повторные операции с учетом прогрессирования НЭК с выведением новой кишечной стомы потребовались у 37% (от 2 до 4 операций).
Закрытие кишечной стомы производили в среднем через 177 дней (20-581, Ме - 189) от момента ее выведения. Средний возраст детей, которым восстанавливали непрерывность кишечника, составлял 25 недель (3-88, Ме - 20,5).
Для определения морфологических изменений отключенной кишки как одного из факторов, лимитирующих время закрытия стомы, изучен биопсийный материал резецированных участков отводящего конца кишечной стомы. Проанализированы морфоструктуры кишечника, оценивались все слои и слизистая оболочка, ее тип, зрелость, степень атрофических изменений, замещение ее фиброзной тканью и очагами ангиоматоза, а также наличие воспалительных изменений.
При исследовании были выявлены следующие изменения: укорочение и отсутствие ворсинок, гиперплазия крипт - данные признаки свидетельствуют об атрофии слизистой оболочки, развившейся в результате нарушения питания кишечной стенки, повреждении нервных волокон в стенке кишки (рисунок 1). В некоторых случаях наблюдали воспалительный инфильтрат, который также способствует развитию в дальнейшем атрофии и фиброза. Об этом свидетельствовало повышенное количество межэпителиальных лимфоцитов, наличие лимфогистиоцитарной инфильтрации в подслизистой оболочке, отек, ангиоматоз и расширение сосудов (рисунок 2). Однако отмечено и наличие признаков возрастного «созревания» структур кишечной стенки.
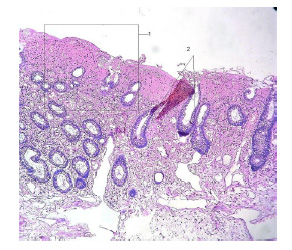
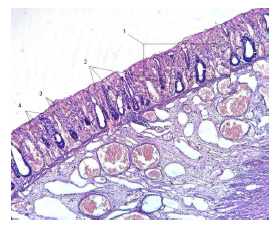
С целью установления зависимости выявленных изменений от других параметров статистическая обработка данных проводилась в программах Statistica 10 и MedCalculator.net с определением коэффициента ранговой корреляции Спирмена. Предварительно была выполнена стандартизация данных по наличию (значение 1) или отсутствию (значение 0) признаков атрофии кишечных структур.
Было установлено, что чем больше времени проходило до операции по восстановлению непрерывности кишечника, тем менее была выражена атрофия слизистой оболочки (р=0,0029). Это обстоятельство связывали с «дозреванием» структур кишечной стенки у недоношенных.
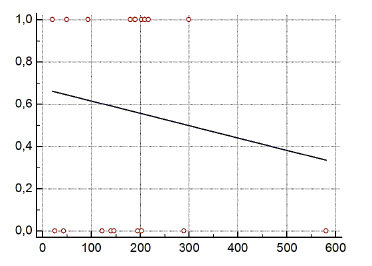
Проведено разделение пациентов в соответствии с 25-75 перцентилями доверительным интервалом от медианы сроков закрытия стомы на группы А - раннее закрытие стомы, срок менее 130 дней; В - среднедлительное закрытие стомы, срок 130-223 дня; и С - позднее закрытие стомы, более 250 дней. В этих группах раннего, среднедлительного и позднего закрытия стомы не получено достоверных данных, подтверждающих различие в сроках первого оперативного лечения. Также не обнаружено достоверной разницы наличия или отсутствия атрофии слизистой оболочки тонкой кишки, и массы тела при рождении. Средняя масса тела пациентов при рождении составила в группе раннего закрытия: 2090,1 г (95% ДИ, 1636,0-2544,2); среднедлительного закрытия: 1974,5 г (95% ДИ, 1410,7-2538,3); позднего закрытия: 2020,0 г. (95% ДИ, 1239,8-2800,1).
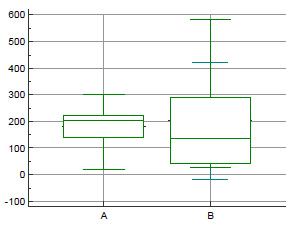
При группировке пациентов по признаку: есть атрофия/нет атрофии кишечной стенки и анализе времени, прошедшем до закрытия стомы, достоверной разницы не выявлено (таблица).
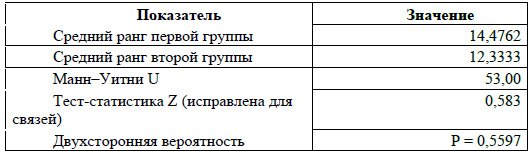
При этом медиана в группе без атрофии значительно ниже (рисунок 4, А - признаки атрофии, В - отсутствие признаков)
При анализе клинических, лабораторных и патоморфологических данных, полученных при выполнении запланированной работы у пациентов, перенесших оперативное лечение по поводу некротизирующего энтероколита и последующего закрытия стом, выявлено следующее:
1. атрофия слизистой оболочки кишечника более выражена у пациентов, которым закрытие кишечной стомы производили с меньшим промежутком времени от первичного вмешательства. Это обстоятельство связывали с «дозреванием» структур кишечной стенки у недоношенных, что является фактором для обоснованного отсроченного закрытия стомы.
1. закрытие кишечной стомы после перенесенного некротизирующего энтероколита нужно выполнять по окончании периода формирования стриктур «отключенной» части кишки (в среднем 3-4 мес.), после ее обязательного рентгенологического контрастного исследования.
Область применения: хирургия.
Рекомендации по использованию: результаты исследования могут быть использованы при хирургическом лечении детей с НЭК.
Предложения по сотрудничеству: консультативная помощь при внедрении.